11月02日,胡刚教授团队与南京医科大学杨硕教授团队的合作研究成果发表在PNAS上在线发表论文“The Gasdermin D N-terminal fragment acts as a negative feedback system to inhibit inflammasome-mediated activation of Caspase-1/11”,该研究揭示了固有免疫细胞焦亡效应分子GSDMD负反馈调控炎症小体激活的新作用和分子机制,为研发靶向炎症小体Caspases的抗炎药物提供了有益的学术基础。我校胡刚教授、王冰微副教授,南京医科大学杨硕教授为该论文共同通讯作者,研究工作得到国家自然科学基金委和科技部重点项目、重大专项等资助。

炎症小体是机体免疫系统中重要的固有免疫炎症蛋白质机器,参与对病原的宿主免疫防御反应,且与无菌性慢性炎症疾病发生密切相关。炎症小体是治疗炎症相关疾病可能的潜在重要靶点,解析炎症小体激活的调控机制对防治炎症性疾病发生具有重要意义。Gasdermin D(GSDMD)是炎症小体下游介导巨噬细胞焦亡的关键效应因子。在病原或体内危险信号刺激下,炎症小体可激活切割GSDMD分子,在质膜表面形成焦亡小孔,进而引发细胞炎性死亡。研究发现,焦亡效应分子GSDMD可通过活化产生的N端片段β1-β2环RFWK基序作用Caspase-1/11酶催化中心,进而控制炎症小体Caspase 的过度激活和炎症反应发生。该研究首次揭示了炎症小体下游的负反馈调控机制,为靶向炎症小体Caspases的抗炎药物开发提供了新线索。
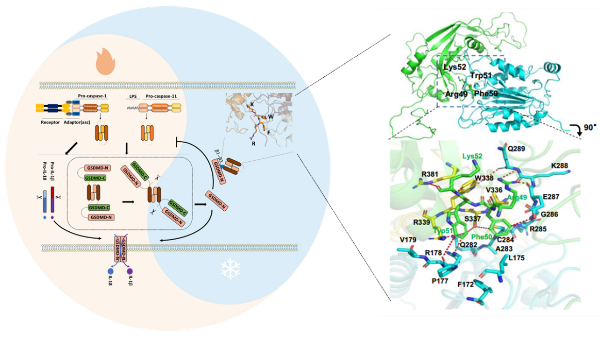
GSDMD负反馈抑制炎症小体Caspases活化

