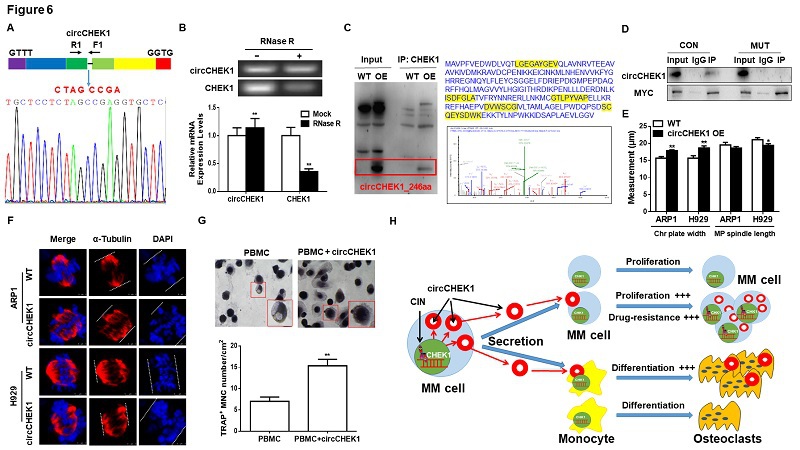
近日,我校医学院•整合医学学院杨烨、顾春艳教授团队先后在 Molecular Cancer、 Journal of Hematology & Oncology 和 Frontiers in Cell and Developmental Biology 等国际知名学术期刊在线发表最新研究成果。 2021 年 6 月 5 日,Springer Nature 旗下 Molecular Cancer 期刊在线发表杨烨、顾春艳 教授课题组题为“ CHEK1 and circCHEK1_246aa evoke chromosomal instability and induce bone lesion formation in multiple myeloma”的文章。该研究首先确定 CHEK1 对多发性骨髓瘤(MM)细胞生长和耐药性的促进作用;还新发现了 circCHEK1_246aa,一种CHEK1环状 RNA,其编码和翻译 MM 细 胞中的 CHEK1 激酶催化中心,并被分泌到 BM 微环境中,促进 MM 增殖和破骨细胞分化;最后,还确定了 CHEK1 新的下游靶基因。 文章首次报道了CHEK1和circCHEK1_246aa 在 MM 发生发展中的调控机制,揭示靶向 CHEK1 和 circCHEK1_246aa 激酶催化中心的 MM 治疗策略具有良好的应用前景。
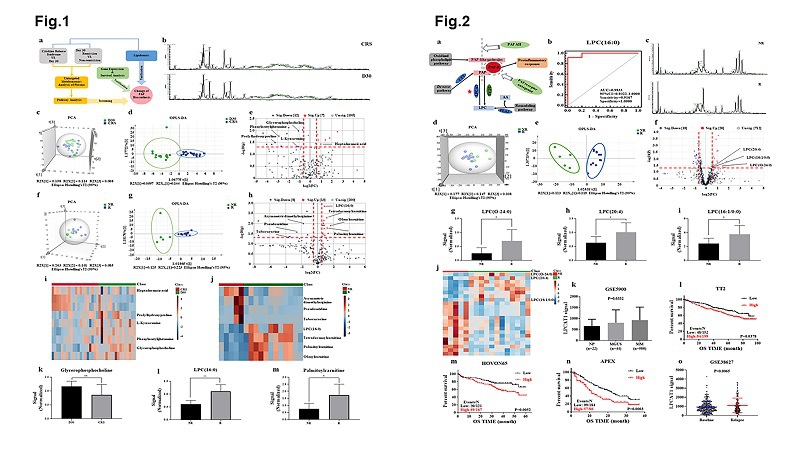
2021 年 6 月 10 日,杨烨、顾春艳教授团队在Journal of Hematology & Oncology 期刊在线发表了题为“CAR-T therapy alters synthesis of platelet-activating factor in multiple myeloma patients”的研究论文。嵌合抗原受体 T 细胞(CAR-T)免疫疗法是一种新型的肿瘤靶向疗法,近年来在复发性或难治性MM 患者中表现出优异疗效。然而,细胞因子释放综合征(CRS)和治疗响应率是限制 CAR-T 应用的主要临床因素。该研究对来自17名接受 CAR-T 治疗的复发或难治性 MM 患者的血浆样品进行了代谢组学和脂质组学分析,探索血浆中用于评估 CRS 和临床疗效的潜在生物标志物,发现两种潜在生物标志物--甘油磷酸胆碱(GPC)和溶血磷脂酰胆碱(LPCs)均参与血小板活化因子(PAF)的合 成。此外,对三个MM的GEP数据集分析发现,调控LPCs合成PAF的关键基因--LPCAT1与 MM 患者不良预后相关。该研究首次报道了CAR-T疗法改变了MM患者体内的PAF合成,CAR-T治疗可能是通过下调LPCAT1的表达抑制PAF合成的再修饰途径,揭示靶向PAF再修饰途径可作为增强CAR-T临床疗效的新策略。
杨烨、顾春艳教授课题组继去年发表的文章“RFWD2 induces cellular proliferation and selective proteasome inhibitor resistance by mediating P27 ubiquitination in multiple myeloma”(Leukemia, 中科院医学一区)首次 证明 RFWD2 是高危 MM 的治疗靶点后,研究团队继续探究RFWD2调控MM细胞增殖、 耐药的作用机制,本研究揭示RFWD2通过与P27的E3泛素连接酶RCHY1相互作用介导P27的泛素化降解,从而影响MM细胞增殖和耐药。

